Nobelgas, någon av de sju kemiska elementen som utgör grupp 18 (VIIIa) i det periodiska systemet. Elementen är helium (He), neon (Ne), argon (Ar), krypton (Kr), xenon (Xe), radon (Rn) och oganesson (Og). De ädla gaserna är färglösa, luktfria, smaklösa, icke brandfarliga gaser. De har traditionellt betecknats grupp 0 i den periodiska tabellen eftersom i årtionden efter deras upptäckt trodde de att de inte kunde binda till andra atomer; det vill säga att deras atomer inte kunde kombineras med andra element för att bilda kemiska föreningar. Deras elektroniska strukturer och upptäckten att vissa av dem verkligen bildar föreningar har lett till en mer lämplig beteckning, grupp 18.
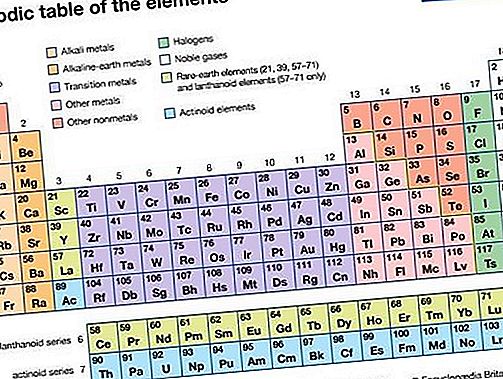
När medlemmarna i gruppen upptäcktes och identifierades, ansågs de vara ytterst sällsynta, såväl som kemiskt inerta, och kallades därför de sällsynta eller inerta gaserna. Det är emellertid känt att flera av dessa element är ganska rikliga på Jorden och i resten av universum, så beteckningen sällsynt är vilseledande. På liknande sätt har användningen av termen inert den nackdelen att den antyder kemisk passivitet, vilket antyder att föreningar från grupp 18 inte kan bildas. Inom kemi och alkemi har ordet ädla länge betecknat motviljan hos metaller, såsom guld och platina, att genomgå kemisk reaktion; det gäller i samma mening för den grupp av gaser som täcks här.
Överflödet av ädelgaserna minskar när deras atomantal ökar. Helium är det mest rikliga elementet i universum utom väte. Alla de ädla gaserna finns i jordens atmosfär och förutom helium och radon är deras huvudsakliga kommersiella källa luften, från vilken de erhålls genom kondensering och fraktionerad destillation. De flesta helium produceras kommersiellt från vissa naturgasbrunnar. Radon isoleras vanligtvis som en produkt av radioaktiv nedbrytning av radiumföreningar. Kärnorna i radiumatomer sönderfaller spontant genom att avge energi och partiklar, heliumkärnor (alfapartiklar) och radonatomer. Vissa egenskaper hos de ädla gaserna listas i tabellen.
Vissa egenskaper hos de ädla gaserna
| helium | neon | argon | krypton | xenon | radon | ununoctium | |
|---|---|---|---|---|---|---|---|
| * Kl. 25.05 atmosfär. | |||||||
| ** hcp = hexagonal nära packad, fcc = ansiktscentrerad kubik (kubik nära packad). | |||||||
| *** Stablest isotop. | |||||||
| atomnummer | 2 | 10 | 18 | 36 | 54 | 86 | 118 |
| atomvikt | 4,003 | 20,18 | 39,948 | 83,8 | 131,293 | 222 | 294 *** |
| smältpunkt (° C) | -272,2 * | -248,59 | -189,3 | -157,36 | -111,7 | -71 | - |
| kokpunkt (° C) | -268,93 | -246,08 | -185,8 | -153,22 | -108 | -61,7 | - |
| densitet vid 0 ° C, 1 atmosfär (gram per liter) | 0,17847 | 0,899 | 1,784 | 3,75 | 5,881 | 9,73 | - |
| löslighet i vatten vid 20 ° C (kubikcentimeter gas per 1 000 gram vatten) | 8,61 | 10,5 | 33,6 | 59,4 | 108,1 | 230 | - |
| isotopisk överflöd (markbunden, procent) | 3 (0,000137), 4 (99,999863) | 20 (90,48), 21 (0,27), 22 (9,25) | 36 (0,3365), 40 (99,6003) | 78 (0,35), 80 (2,28), 82 (11,58), 83 (11,49), 84 (57), 86 (17,3) | 124 (0,09), 126 (0,09), 128 (1,92), 129 (26,44), 130 (4,08), 131 (21,18), 132 (26,89), 134 (10,44), 136 (8,87) | - | - |
| radioaktiva isotoper (massantal) | 5-10 | 16–19, 23–34 | 30–35, 37, 39, 41–53 | 69–77, 79, 81, 85, 87–100 | 110–125, 127, 133, 135–147 | 195-228 | 294 |
| färg på ljus som avges från gasformigt urladdningsrör | gul | röd | röd eller blå | gulgrön | blå till grön | - | - |
| fusionsvärme (kilojoules per mol) | 0,02 | 0,34 | 1,18 | 1,64 | 2,3 | 3 | - |
| förångningsvärme (kalorier per mol) | 0,083 | 1,75 | 6,5 | 9,02 | 12,64 | 17 | - |
| specifik värme (joule per gram Kelvin) | 5,1931 | 1,03 | 0,52033 | 0,24805 | 0,15832 | 0,09365 | - |
| kritisk temperatur (K) | 5,19 | 44,4 | 150,87 | 209,41 | 289,77 | 377 | - |
| kritiskt tryck (atmosfärer) | 2,24 | 27,2 | 48,34 | 54,3 | 57,65 | 62 | - |
| kritisk densitet (gram per kubikcentimeter) | 0,0696 | 0,4819 | 0,5356 | 0,9092 | 1,103 | - | - |
| värmeledningsförmåga (watt per meter Kelvin) | 0,1513 | 0,0491 | 0,0177 | 0,0094 | 0,0057 | 0,0036 | - |
| magnetisk känslighet (cgs-enheter per mol) | -0,0000019 | -0,0000072 | -0,0000194 | -0,000028 | -0,000043 | - | - |
| kristallstruktur** | hcp | fcc | fcc | fcc | fcc | fcc | - |
| radie: atom (ångström) | 0,31 | 0,38 | 0,71 | 0,88 | 1,08 | 1,2 | - |
| radie: kovalent (kristall) uppskattad (ångström) | 0,32 | 0,69 | 0,97 | 1,1 | 1,3 | 1,45 | - |
| statisk polariserbarhet (kubiska ångström) | 0,204 | 0,392 | 1,63 | 2,465 | 4,01 | - | - |
| joniseringspotential (först, elektron volt) | 24,587 | 21,565 | 15,759 | 13,999 | 12,129 | 10,747 | - |
| elektronegativitet (Pauling) | 4,5 | 4,0 | 2,9 | 2,6 | 2,25 | 2,0 | - |










![Strid om Falklandsöarna första världskriget [1914] Strid om Falklandsöarna första världskriget [1914]](https://images.thetopknowledge.com/img/world-history/7/battle-falkland-islands-world-war-i-1914.jpg)
