Anhydrid, vilken kemisk förening som erhålls antingen i praktiken eller i princip genom eliminering av vatten från en annan förening. Exempel på oorganiska anhydrider är svaveltrioxid, SO 3, som härrör från svavelsyra, och kalciumoxid, CaO, härrörande från kalciumhydroxid. Svaveltrioxid och andra oxider som bildas genom avlägsnande av vatten från en syra kallas ofta syraanhydrider, medan de som kalciumoxid som produceras av en bas vid förlust av vatten betecknas basiska anhydrider.
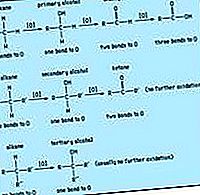
karboxylsyra: Anhydrider
Den funktionella gruppen av en karboxylsyraanhydrid är två acylgrupper bundna till en syreatom. Anhydriden kan vara symmetrisk (två identiska
Den viktigaste av de organiska anhydrider är ättiksyraanhydrid, (CH 3 CO) 2 O. Den framställs industriellt i endera av två sätt: genom atmosfärisk oxidation av acetaldehyd i närvaro av en metall acetat; och från ättiksyra genom reaktion med acetylen eller keten. Andra organiska anhydrider kan framställas från karboxylsyror genom reaktion med ättiksyraanhydrid, keten, metoxiacetylen eller isopropenylacetat. Anhydrider produceras också när acylhalogenider reagerar med ättiksyraanhydrid eller med karboxylsyra och pyridin.
De organiska anhydriderna används för att introducera acylgruppen (RCO) i organisk syntes. De reagerar med vatten för att ge karboxylsyror, med alkoholer eller fenoler för att ge estrar och med ammoniak och aminer för att ge amider. Ättiksyraanhydrid används vid tillverkning av cellulosaacetat, som ofta används som bas för magnetband och vid tillverkning av textilfibrer. Dessutom värms den upp med salicylsyra för att producera den medicinska kemiska acetylsalicylsyra (aspirin).