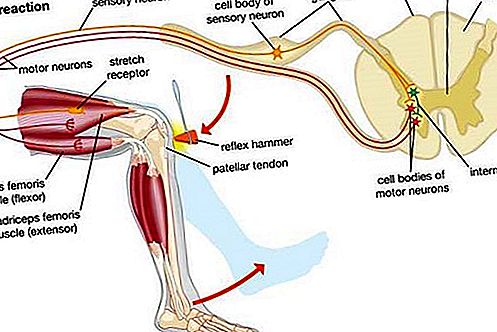
Cryopreservation, bevarande av celler och vävnad genom frysning.

Sir Ian Wilmut: Utbildning och kryokonserveringsforskning
Wilmut växte upp i Coventry, en stad i det historiska engelska länet Warwickshire, och han gick på jordbrukshögskolan vid universitetet
Cryopreservation baseras på förmågan hos vissa små molekyler att komma in i celler och förhindra dehydrering och bildning av intracellulära iskristaller, vilket kan orsaka celldöd och förstörelse av cellorganeller under frysprocessen. Två vanliga kryoprotektiva medel är dimetylsulfoxid (DMSO) och glycerol. Glycerol används främst för kryobeskyddande av röda blodkroppar, och DMSO används för att skydda de flesta andra celler och vävnader. Ett socker som kallas trehalos, som förekommer i organismer som kan överleva extrem uttorkning, används för frystorkningsmetoder för kryokonservering. Trehalos stabiliserar cellmembran, och det är särskilt användbart för bevarande av spermier, stamceller och blodceller.
De flesta system för cellulär kryokonservering använder en frys med kontrollerad hastighet. Detta fryssystem levererar flytande kväve i en stängd kammare i vilken cellsuspensionen placeras. Noggrann övervakning av frysningshastigheten hjälper till att förhindra snabb celluttorkning och bildning av iskristall. I allmänhet tas cellerna från rumstemperatur till ungefär -90 ° C (-130 ° F) i en frys med kontrollerad hastighet. Den frysta cellsuspensionen överförs sedan till en frys-kvävefrysare som hålls vid extremt kalla temperaturer med kväve i antingen ånga eller flytande fas. Kryopreservering baserat på frystorkning kräver inte användning av fryst-kväve frysar.
En viktig tillämpning av kryokonservering är frysning och lagring av hematopoietiska stamceller, som finns i benmärgen och perifert blod. Vid autolog räddning av benmärg samlas hematopoietiska stamceller från en patients benmärg före behandling med högdoskemoterapi. Efter behandlingen tinas upp patientens kryokonserverade celler och infunderas tillbaka i kroppen. Denna procedur är nödvändig eftersom högdoskemoterapi är extremt giftig för benmärgen. Förmågan att kryopreservera hematopoietiska stamceller har förbättrat utfallet för behandling av vissa lymfom och maligniteter i fast tumör. När det gäller patienter med leukemi är deras blodkroppar cancer och kan inte användas för autolog benmärgsräddning. Som ett resultat förlitar sig dessa patienter på kryokonserverat blod som samlats in från navelsträngarna hos nyfödda barn eller på kryokonserverade hematopoietiska stamceller erhållna från givare. Sedan slutet av 1990-talet har man insett att hematopoietiska stamceller och mesenkymala stamceller (härledda från embryonal bindväv) är kapabla att differentiera sig i skelett- och hjärtmuskelvävnader, nervvävnad och ben. Idag finns det ett intensivt intresse för tillväxten av dessa celler i vävnadskultursystem, liksom för kryokonservering av dessa celler för framtida terapi för en mängd olika störningar, inklusive störningar i nerv- och muskelsystem och sjukdomar i levern och hjärtat..
Cryopreservation används också för att frysa och lagra mänskliga embryon och spermier. Det är särskilt värdefullt för frysning av extra embryon som genereras genom in vitro-befruktning (IVF). Ett par kan välja att använda cyropreserverade embryon för senare graviditeter eller i händelse av att IVF misslyckas med färska embryon. I processen med fryst embryotransfer tines embryon upp och implanteras i kvinnans livmodern. Fryst embryoöverföring är associerat med en liten men betydande ökning av risken för barncancer bland barn födda från sådana embryon.
Djup hypotermi, en form av mild kryokonservering som används hos mänskliga patienter, har betydande tillämpningar. En vanlig användning av induktion av djup hypotermi är för komplexa kardiovaskulära kirurgiska ingrepp. Efter att patienten har placerats på en fullständig kardiopulmonal bypass, med hjälp av en hjärta-lungmaskin, passerar blodet genom en kylkammare. Kontrollerad kylning av patienten kan nå extremt låga temperaturer på cirka 10–14 ° C (50–57 ° F). Denna mängd kylning stoppar effektivt all cerebral aktivitet och ger skydd för alla vitala organ. När denna extrema kylning har uppnåtts kan hjärt-lungmaskinen stoppas och kirurgen kan korrigera mycket komplexa aorta- och hjärtfel under cirkulationsstopp. Under denna tid cirkulerar inget blod inom patienten. Efter operationen värms blodet gradvis i samma värmeväxlare som används för kylning. Gradvis uppvärmning tillbaka till normala kroppstemperaturer resulterar i återupptagande av normala hjärn- och organfunktioner. Denna djupa hypotermi är emellertid långt borta från frysning och långvarig kryokonservering.
Cellerna kan leva mer än ett decennium om de är korrekt frysta. Dessutom kan vissa vävnader, såsom parathyroidkörtlar, vener, hjärtventiler och aortavävnad framgångsrikt kryokonserveras. Frysning används också för att lagra och upprätthålla långsiktig livskraft för tidiga mänskliga embryon, ägg (ägg) och spermier. Frysningsförfarandena som används för dessa vävnader är väl etablerade, och i närvaro av kryo-skyddande medel kan vävnaderna förvaras under långa tidsperioder vid temperaturer på -14 ° C (6,8 ° F).
Forskning har visat att hela djur som är frysta i frånvaro av kryoprotektiva medel kan ge livskraftiga celler som innehåller intakt DNA vid upptining. Till exempel har kärnor i hjärnceller från hela möss lagrade vid -20 ° C (-4 ° F) i mer än 15 år använts för att generera linjer med embryonala stamceller. Dessa celler användes därefter för att producera muskloner.




![Dial M for Murder film av Hitchcock [1954] Dial M for Murder film av Hitchcock [1954]](https://images.thetopknowledge.com/img/entertainment-pop-culture/7/dial-m-murder-film-hitchcock-1954.jpg)