Salpetersyra, (HNO 3), färglös, rökande och mycket frätande vätska (fryspunkt −42 ° C [−44 ° F], kokpunkt 83 ° C [181 ° F]) som är ett vanligt laboratoriereagens och ett viktigt industrikemikalie för tillverkning av gödselmedel och sprängämnen. Det är giftigt och kan orsaka svåra brännskador.
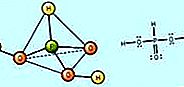
oxysyra: Salpetersyra och nitratsalter
Salpetersyra, HNO3, var känd för alkemisterna på 800-talet som ”aqua fortis” (starkt vatten). Det bildas
Beredningen och användningen av salpetersyra var känd för de tidiga alkemisterna. En vanlig laboratorieprocess som använts under många år, tillskriven en tysk kemist, Johann Rudolf Glauber (1648), bestod av att värma kaliumnitrat med koncentrerad svavelsyra. 1776 visade Antoine-Laurent Lavoisier att den innehöll syre och 1816 etablerade Joseph-Louis Gay-Lussac och Claude-Louis Berthollet sin kemiska sammansättning.
Den huvudsakliga metoden för framställning av salpetersyra är den katalytiska oxidationen av ammoniak. I den metod som utvecklats av den tyska kemisten Wilhelm Ostwald 1901 oxideras successivt ammoniakgas till kväveoxid och kvävedioxid med luft eller syre i närvaro av en platina-gasskatalysator. Kvävedioxiden absorberas i vatten för att bilda salpetersyra. Den resulterande syra-i-vatten-lösningen (cirka 50-70 viktprocent syra) kan dehydratiseras genom destillation med svavelsyra.
Salpetersyra sönderdelas i vatten, kvävedioxid och syre och bildar en brungul lösning. Det är en stark syra, fullständigt joniserad i hydronium (H 3 O +) och nitrat (NO 3 -) joner i vattenlösning, och en kraftfull oxidationsmedel (en som fungerar som elektronmottagare i oxidations-reduktionsreaktioner). Bland de många viktiga reaktionerna av salpetersyra är: neutralisering med ammoniak för att bilda ammoniumnitrat, en viktig del av gödselmedel; nitrering av glycerol och toluen, bildande sprängämnena nitroglycerin respektive trinitrotoluen (TNT); framställning av nitrocellulosa; och oxidation av metaller till motsvarande oxider eller nitrater.