Xenon (Xe), kemiskt element, en tung och extremt sällsynt gas från grupp 18 (ädla gaser) i det periodiska systemet. Det var den första ädelgasen som hittades för att bilda verkliga kemiska föreningar. Mer än 4,5 gånger tyngre än luft är xenon färglös, luktfri och smaklös. Fast xenon tillhör det ansiktscentrerade kubiska kristallsystemet, vilket innebär att dess molekyler, som består av enstaka atomer, uppför sig som sfärer packade ihop så nära som möjligt. Namnet xenon härrör från det grekiska ordet xenos, "konstigt" eller "främmande."

ädelgas
(Ar), krypton (Kr), xenon (Xe), radon (Rn) och oganesson (Og). De ädla gaserna är färglösa, luktfria, smaklösa, icke brandfarliga gaser.
.Elementegenskaper
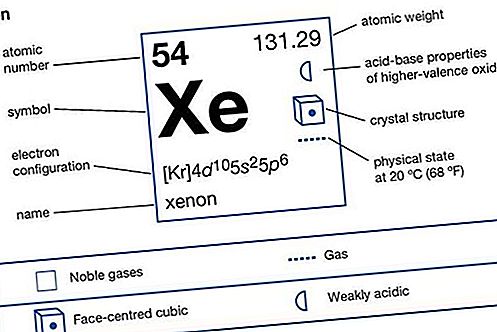
| atomnummer | 54 |
|---|---|
| atomvikt | 131,29 |
| smältpunkt | −111,9 ° C (−169,4 ° F) |
| kokpunkt | −108.0 ° C (−162.4 ° F) |
| densitet (1 atm, 0 ° C [32 ° F]) | 5,887 g / liter (0,078 ounce / gallon) |
| oxidationstillstånd | 0, +2, +4, +6, +8 |
| elektronkonfigur. | (Kr) 4d 10 5s 2 5p 6 |
Elementets egenskaper
Xenon förekommer i små spår i gaser inom jorden och är närvarande i en utsträckning av cirka 0,0000086 procent, eller cirka 1 del i 10 miljoner volym torr luft. Liksom flera andra ädla gaser finns xenon i meteoriter. Xenon tillverkas i liten skala genom fraktionerad destillation av flytande luft. Det är den minst flyktiga (kokpunkten, −108,0 ° C [−162,4 ° F]) för de ädla gaserna som kan erhållas från luften. De brittiska kemisterna Sir William Ramsay och Morris W. Travers isolerade elementet 1898 genom upprepad fraktionerad destillation av krypturen av ädelgas som de hade upptäckt sex veckor tidigare.
Elementet xenon används i lampor som producerar extremt korta och intensiva ljusblinkar, till exempel stroboskop och ljus för höghastighetsfotografering. När en laddning av elektricitet passeras genom gasen vid lågt tryck, avger den en blixt av blåvit-ljus vid högre tryck avges vitt ljus som liknar dagsljus. Xenon ficklampor används för att aktivera rubinlasrar.
Naturlig xenon är en blandning av nio stabila isotoper i följande procentsatser: xenon-124 (0,096), xenon-126 (0,090), xenon-128 (1,92), xenon-129 (26,44), xenon-130 (4,08), xenon -131 (21,18), xenon-132 (26,89), xenon-134 (10,44) och xenon-136 (8,87). Massantalet för de kända isotoperna av xenon sträcker sig från 118 till 144. Xenonen som finns i vissa steniga meteoriter visar en stor andel av xenon-129, tros vara en produkt av radioaktivt förfall av jod-129, vars halveringstid är 17 000 000 år. Att mäta xenon-129-innehållet i meteoriter belyser solsystemets historia. Mer än ett dussin radioaktiva xenonisotoper producerade genom klyvning av uran och andra kärnreaktioner är kända. Exempelvis produceras xenon-135 (9,2 timmars halveringstid) genom uranavsplitning i kärnreaktorer, där det är besvärligt eftersom det absorberar fission-producerande neutroner. Xenon-129 är av speciell betydelse eftersom denna isotop kan observeras genom kärnmagnetisk resonansspektroskopi, vilket gör det användbart för strukturell karakterisering av xenonföreningar. De xenonisotoper som produceras i den största mängden genom kärnklyvning är xenon-131, -132, -134 och -136, som är stabila, och xenon-133, som är radioaktiv, med en halveringstid på 5,27 dagar.




![Dial M for Murder film av Hitchcock [1954] Dial M for Murder film av Hitchcock [1954]](https://images.thetopknowledge.com/img/entertainment-pop-culture/7/dial-m-murder-film-hitchcock-1954.jpg)