Oxysyra, vilken syreinnehållande syra som helst. De flesta kovalenta icke-metalliska oxider reagerar med vatten och bildar sura oxider; det vill säga, reagerar de med vatten för att bilda oxisyror att utbytet hydroniumjoner (H 3 O +) i lösning. Det finns vissa undantag, såsom kolmonoxid, CO, dikväveoxid, N 2 O och kväveoxid, NO.
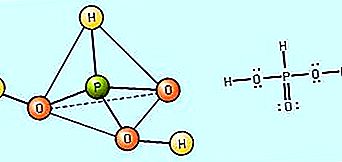
Styrken hos en oxysyra definieras av i vilken utsträckning den dissocieras i vatten (dvs dess förmåga att bilda H + -joner). I allmänhet kan oxysyras relativa styrka förutsägas på grundval av elektronegativiteten och oxidationsnumret för den centrala icke-metala atomen. Syrahållfastheten ökar när elektronatomen hos centralatomen ökar. Eftersom exempelvis klor (Cl) elektronegativitet är större än svavel (S), som i sin tur är större än fosfor (P), kan det förutsägas att perklorsyra, HClO 4, är en starkare syra än svavelsyra, H 2 SO 4, som bör vara en starkare syra än fosforsyra, H 3 PO 4. För en given icke-metallisk centralatom ökar syrestyrkan när oxidatorn för centralatomen ökar. Till exempel är salpetersyra, HNO 3, i vilken kväveatomen (N) har ett oxidationsantal på +5, en starkare syra än salpetersyra, HNO 2, där kväveoxidationstillståndet är +3. På samma sätt, svavelsyra, H 2 SO 4, med svavel i dess sex oxidationstillstånd, är en starkare syra än svavelsyrlighet, H 2 SO 3, där en 4 oxidationstal av svavel föreligger.
Saltet av en oxysyra är en förening som bildas när syran reagerar med en bas: syra + bas → salt + vatten. Denna typ av reaktion kallas neutralisering, eftersom lösningen görs neutral.