Thorium (Th), radioaktivt kemiskt element i actinoid-serien i det periodiska systemet, atomnummer 90; det är ett användbart kärnreaktorbränsle. Thorium upptäcktes (1828) av den svenska kemisten Jöns Jacob Berzelius. Det är silvigt vitt men blir grått eller svart vid exponering för luft. Det är ungefär hälften så rikligt som bly och är tre gånger mer rikligt än uran i jordskorpan. Thorium återvinns kommersiellt från mineralen monazit och förekommer också i andra mineraler som torit och thorianit. Torium metall har framställts i kommersiella kvantiteter genom reduktion av tetrafluorid (ThF 4) och dioxid (ThO 2) och genom elektrolys av tetraklorid (THCl 4). Elementet fick sitt namn efter den norska guden Thor.

actinoid element: Praktiska tillämpningar av actinoiderna
Thorium är också potentiellt av stort ekonomiskt värde eftersom en av dess isotoper, thorium-232, kan omvandlas till
Metallen kan strängsprutas, valsas, smiddas, svängas och snurras, men ritningen är svår på grund av thoriums låga draghållfasthet. Denna och andra fysiska egenskaper såsom smält- och kokpunkter påverkas starkt av små mängder av vissa föroreningar, såsom koldioxid och toriumdioxid. Thorium sättes till magnesium- och magnesiumlegeringar för att förbättra deras höga temperaturhållfasthet. Det har använts i kommersiella fotoelektriska celler för att mäta ultraviolett ljus med våglängder som sträcker sig från 2000 till 3750 ångström. Tillsatt till glas ger thorium glas med högt brytningsindex, användbart för specialiserade optiska applikationer. Det var tidigare mycket efterfrågat som en komponent i mantlar för gas- och fotogenlampor och har använts för tillverkning av volframfilament för glödlampor och vakuumrör.
Thoriums radioaktivitet hittades oberoende (1898) av den tyska kemisten Gerhard Carl Schmidt och av den franska fysikern Marie Curie. Naturligt thorium är en blandning av radioaktiva isotoper, främst den mycket långlivade thorium-232 (1,40 × 10 10- års halveringstid), förälder till den radioaktiva förfallsserien av thorium. Andra isotoper förekommer naturligt i uran- och aktiniumförfallsserien, och thorium finns i alla uranmalmer. Thorium-232 är användbar i uppfödningsreaktorer eftersom den fångar långsamma neutroner nedbrytes till klyvbart uran-233. Syntetiska isotoper har framställts; thorium-229 (7 880 års halveringstid), bildad i sönderfallskedjan med ursprung i det syntetiska actinoidelementet neptunium, fungerar som en spårämne för vanligt thorium (thorium-232).
Thorium uppvisar ett oxidationstillstånd på +4 i nästan alla dess föreningar. Th 4+ jonen bildar många komplexa joner. Dioxiden (ThO 2), ett mycket eldfast ämne, har många industriella tillämpningar; thoriumnitrat har funnits som ett kommersiellt salt.
Elementegenskaper
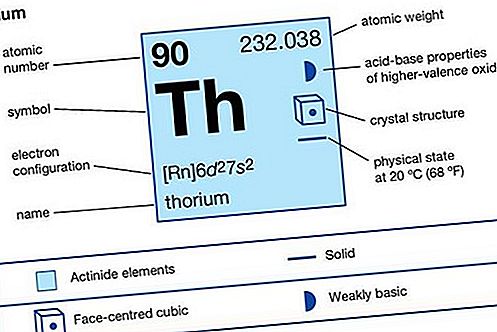
| atomnummer | 90 |
|---|---|
| atomvikt | 232,038 |
| smältpunkt | cirka 1 700 ° C (3,100 ° F) |
| kokpunkt | cirka 4000 ° C (7 200 ° F) |
| Specifik gravitation | cirka 11,66 (17 ° C) |
| oxidationstillstånd | 4 |
| elektronkonfiguration av gasformigt atomtillstånd | [Rn] 6d 2 7s 2 |








![Kansas-Nebraska Act United States [1854] Kansas-Nebraska Act United States [1854]](https://images.thetopknowledge.com/img/politics-law-government/7/kansas-nebraska-act-united-states-1854.jpg)




