Tillsats av kolnukleofiler
En stor mängd kolnukleofiler lägger till aldehyder, och sådana reaktioner är av största vikt i syntetisk organisk kemi eftersom produkten är en kombination av två kolskelett. Organiska kemister har kunnat sätta ihop nästan vilket som helst kolskelett, oavsett hur komplicerat, genom genial användning av dessa reaktioner. En av de äldsta och viktigaste är tillsatsen av Grignard-reagens (RMgX, där X är en halogenatom). Den franska kemisten Victor Grignard vann Nobelpriset i kemi 1912 för upptäckten av dessa reagenser och deras reaktioner.
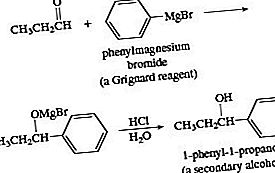
Tillsats av ett Grignard-reagens till en aldehyd följt av surgöring i vattenhaltig syra ger en alkohol. Tillsats till formaldehyd ger en primär alkohol. Tillsats till en annan aldehyd än formaldehyd ger en sekundär alkohol.
En annan kolnukleofil är cyanidjonen, CN -, som reagerar med aldehyder för att efter försurning ge cyanohydriner, föreningar innehållande en OH- och CN-grupp på samma kolatom.
Benzaldehyd cyanohydrin (mandelonitril) ger ett intressant exempel på en kemisk försvarsmekanism i den biologiska världen. Detta ämne syntetiseras av tusenbehållare (Apheloria corrugata) och lagras i speciella körtlar. När ett tusenbein hotas utsöndras cyanohydrinet från sin lagringskörtlar och genomgår enzymkatalyserad dissociation för att producera vätecyanid (HCN). Millipeden frigör sedan HCN-gasen i dess omgivning för att avvärja rovdjur. Mängden HCN som släpps ut av en enda tusenbehållare är tillräcklig för att döda en liten mus. Mandelonitril finns också i bittra mandlar och persika gropar. Dess funktion där är okänd.
Andra viktiga reaktioner i denna kategori inkluderar Knoevenagel-reaktionen, i vilken kolnukleofilen är en ester med minst en a-väte. I närvaro av en stark bas förlorar estern ett a-väte för att ge ett negativt laddat kol som sedan tillför karbonylkolet i en aldehyd. Försurning följt av förlust av en vattenmolekyl ger en a, p-omättad ester.
En annan tilläggsreaktion som involverar en kolnukleofil är Wittig-reaktionen, i vilken en aldehyd reagerar med en fosforan (även kallad fosforylid) för att ge en förening som innehåller en kol-kol-dubbelbindning. Resultatet av en Wittig-reaktion är ersättningen av karbonylsyran i en aldehyd med kolgruppen bunden till fosfor. Den tyska kemisten Georg Wittig delade 1979 Nobelpriset i kemi för upptäckten av denna reaktion och utvecklingen av dess användning i syntetisk organisk kemi.
Föreningar innehållande en trimetylsilylgrupp (-SiMe 3, där Me är metylgruppen, -CH 3) och en litium (Li) atom på samma kolatom reagerar med aldehyder i den så kallade Peterson reaktion för att ge samma produkter som skulle kan erhållas genom en motsvarande Wittig-reaktion.
Förskjutning vid a-kolet
α-Halogenering
En α-väte av en aldehyd kan ersättas av en klor (Cl), brom (Br) eller jod (I) atom när föreningen behandlas med Cl 2, Br 2 eller I 2, respektive, antingen utan en katalysator eller i närvaro av en sur katalysator.
Reaktionen kan lätt stoppas efter att endast en halogenatom tillsatts a-halogenering sker faktiskt på enolformen (se ovan Egenskaper för aldehyder: Tautomerism) hos aldehyden snarare än på själva aldehyden. Samma reaktion inträffar om en bas tillsätts, men då kan den inte stoppas förrän alla a-halogener som är fästa vid samma kol har ersatts med halogenatomer. Om det finns tre a-väten på samma kol, går reaktionen ett steg längre, vilket resulterar i klyvning av en X 3 C - jon (där X är en halogen) och bildningen av saltet av en karboxylsyra.

Denna reaktion kallas haloformreaktionen, eftersom X 3 C - joner reagerar med vatten eller en annan syra närvarande i systemet för att framställa föreningar med formen X 3 CH, vilka kallas haloforms (t.ex. CHCl 3 kallas kloroform).